2006 (613)
2007 (556)
2008 (369)
2009 (298)
2011 (232)
2012 (174)
2013 (145)
2014 (89)
2015 (101)
2016 (83)
2017 (53)
2019 (76)
2021 (62)
2022 (116)
2023 (95)

美国食品药品管理局(FDA)的专家小组一致同意,批准一款名为lecanemab的药物,用于临床治疗阿尔茨海默氏病(也被称为“老年痴呆症”)。
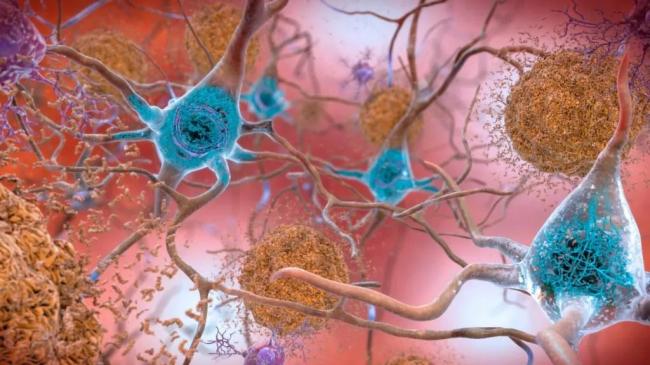
这意味着,这种以 Leqembi品牌销售的药物应该会在7月6日之前获得 FDA的全面批准,美国650万患有老年痴呆症的病人有望获得首批药物。至于其他国家,有些全部采用FDA标准的国家也能得到药物,而有些自己有类似官方机构的国家,则要自己评估再决定是否引进这种药物。
与所有药物一样,lecanemab在FDA的监管下进行了大型的双盲试验,该实验招募了800多名早期老年痴呆症患者,并测试了不同剂量的 Leqembi所产生的效果。结果表明,在18个月的试验周期里,使用了lecanemab进行治疗的患者,与安慰剂相比,轻度认知障碍或阿尔茨海默氏痴呆患者的认知能力下降速度要慢27%。
在生活表现来看,接受lecanemab治疗的患者,在日常生活中的表现也优于安慰剂的患者,比如自己穿衣服和吃饭。
FDA在今年年初批准了该药物的紧急使用授权,在经过半年的临床试验后,FDA专家确认该药物的确对老年痴呆症患者有益,因此全面批准了lecanemab在美国上市,按照程序,有望在7月6日之前拿到正式批文。
 不过,控制医疗保险的医疗保险和医疗补助服务中心表示,只会为在国家登记处注册的患者提供该药物,而如何注册成为难题。
不过,控制医疗保险的医疗保险和医疗补助服务中心表示,只会为在国家登记处注册的患者提供该药物,而如何注册成为难题。
美国阿尔茨海默氏症协会抨击这种官僚主义的做法,称该障碍“是不必要的且可能有害的障碍”。
“医疗保险应该是美国人的坚如磐石的保证,现在是“医疗保险和医疗补助服务中心”加强并在 FDA传统批准之日提供医疗保险访问的时候了。”阿尔茨海默氏症协会在一份声明中说声明,“患有阿尔茨海默氏病的美国人应该无障碍地获得 FDA批准的治疗,就像患有癌症、心脏病和艾滋病毒/艾滋病的人一样。”该倡导组织补充说。



